Tensioattivi e detergenza
Pubblicato da cosmetimag il

Indice
ToggleTensioattivi e detergenza
La scelta di detergenti adatti al proprio tipo di pelle ed alle proprie esigenze è molto importante per mantenere la cute in buono stato. I detergenti infatti hanno lo scopo di rimuovere lo sporco, il sebo, il sudore, i microrganismi e le cellule morte, ma possono essere causa di micro-aggressioni verso la pelle e della perdita di lipidi e proteine dello strato corneo.
Cosa sono i tensioattivi
I tensioattivi sono molecole in grado di ridurre la tensione interfacciale, ovvero l’energia coesiva tra le molecole di acqua che vengono in contatto con un altro liquido, con l’aria o con un solido. Sulla pelle sono in grado di rimuovere lo sporco solubilizzandolo in strutture dette micelle che vengono asportate con il risciacquo.
Dal punto di vista chimico i tensioattivi sono molecole anfipatiche, ovvero molecole che presentano sia gruppi polari che gruppi apolari. Per dirlo in parole semplici, possiamo immaginarli con una testa affine all’acqua ed una coda affine agli oli. Questa caratteristica è fondamentale per il loro meccanismo d’azione. In presenza di olio e acqua infatti i tensioattivi si posizionano all’interfaccia tra i due, con la testa (affine all’acqua) in acqua e la coda (affine ai lipidi) nella fase oleosa.

Meccanismo d'azione dei tensioattivi - formazione delle micelle
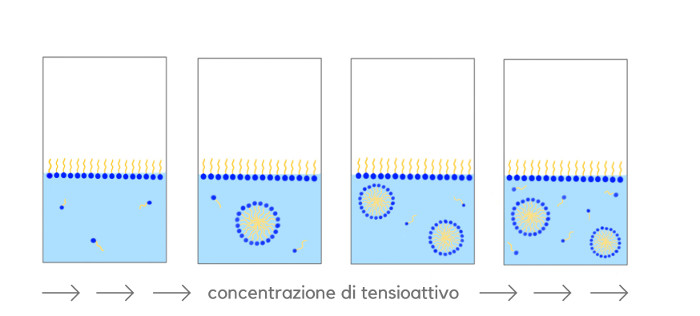
A basse concentrazioni i tensioattivi in acqua si posizionano con le teste idrofiliche sul pelo dell’acqua e le code all’esterno.
Aumentando la concentrazione di tensioattivo le molecole riempiono l’interfaccia acqua-aria e acqua-recipiente ed iniziano a disperdersi casualmente nell’acqua sotto forma di monomeri liberi.
Aggiungendo ancora tensioattivo alla soluzione si raggiunge la cosiddetta concentrazione micellare critica (CMC), concentrazione alla quale i tensioattivi iniziano ad aggregarsi in micelle. Le micelle sono strutture sferiche composte da tensioattivi che hanno la testa idrofila (affine all’acqua) esternamente e la coda lipofila (affine agli oli, che non va d’accordo con l’acqua) all’interno. Lo sporco, che è lipofilo, è affine alle code e tra queste viene intrappolato. Con il risciacquo le micelle e lo sporco vengono rimossi. Quindi è oltre la concentrazione micellare critica che i tensioattivi presentano proprietà lavanti.

Aumentando la concentrazione di tensioattivo oltre la CMC aumenta il numero delle micelle. Oltre una certa concentrazione però non aumenta l’effetto lavante ma aumentano i monomeri liberi e quindi il rischio di irritazione cutanea è maggiore, poiché i monomeri liberi, a differenza delle micelle, possono penetrare lnela cute, denaturare la cheratina e danneggiare la barriera cutanea. Il danneggiamento della barriera cutanea si manifesta con irritazione, discomfort, rossori, secchezza.
Proprietà dei tensioattivi
Per le loro caratteristiche chimiche i tensioattivi hanno diversi effetti positivi o desiderabili nei cosmetici:
– effetto pulente: emulsionano lo sporco che così può essere rimosso con il risciacquo.
– produzione di schiuma
– effetto bagnante: i tensioattivi aumentano la superficie di contatto tra l’acqua ed un substrato (ad esempio la pelle)
– effetto emulsionante e solubilizzante
Bisogna però tenere presente che i tensioattivi possono anche avere effetti negativi come l’aumento del pH cutaneo (tipico dei saponi classici), il danneggiamento delle proteine, l’asportazione di lipidi di membrana. Possono essere anche risultare irritanti e sensibilizzanti in certe condizioni.
Classificazione dei tensioattivi
I tensioattivi si possono classificare in base alla carica presente sulla testa cationica in 4 gruppi: anionici, cationici, anfoteri, non ionici.
• TENSIOATTIVI ANIONICI
I tensioattivi anionici hanno una carica negativa sulla testa idrofila. Questi tensioattivi hanno un elevato potere pulente, buone proprietà bagnanti, un ottimo potere schiumogeno e moderata azione disinfettante ma hanno anche un elevato potere irritante. I tensioattivi anionici etossilati sono generalmente meno irritanti.
Esempi: sodio lauril solfato (o SLS, INCI: sodium lauryl sulfate), sodio lauril etossisolfato (o SLES, INCI: sodium laureth sulfate).
• TENSIOATTIVI CATIONICI
I tensioattivi cationici hanno una carica positiva sulla testa idrofila. Questi tensioattivi hanno minori proprietà detergenti rispetto ai tensioattivi anionici e fanno meno schiuma ma sono più attivi verso i microrganismi. La presenza della carica positiva li rende utilizzabili come condizionanti ed agenti antistatici nei prodotti per capelli.
Esempi: benzalconio cloruro (INCI: benzalkonium chloride)
• TENSIOATTIVI ANFOTERI
I tensioattivi anfoteri presentano entrambe le cariche + e – sulla testa idrofila. Hanno un buon potere detergente e schiumogeno e moderata attività antimicrobica. Sono meno aggressivi dei tensioattivi anionici e per questo sono usati in combinazione con essi per ottenere prodotti più delicati.
Esempi: cocamidopropil betaina (INCI: cocamidopropyl betaine), sodium cocoamphodiacetate
• TENSIOATTIVI NON IONICI
I tensioattivi non ionici non hanno alcuna carica sulla testa idrofila. Questi tensioattivi hanno scarso potere detergente e scarso potere schiumogeno e sono estremamente delicati. Sono usati anche come emulsionanti e viscosizzanti.
Esempi: coco glucosyde, lauryl glucoside, cocamide DEA.
Scegliere un detergente delicato
Abbiamo visto che i tensioattivi non sono tutti uguali e che alcuni sono più irritanti di altri, ma abbiamo anche visto che il potere irritante di un tensioattivo dipende dalla concentrazione micellare critica e dalla concentrazione del tensioattivo. Non è semplice capire la delicatezza o l’aggressività di un detergente solo leggendo la lista degli ingredienti. La presenza di tensioattivi delicati può essere un indizio ma non una certezza.
Inoltre la delicatezza di un detergente è una caratteristica soggettiva, che dipende fortemente dal tipo di pelle.
Nella ricerca di un detergente delicato fate affidamento all’etichetta dei cosmetici e cercate le diciture “detergente delicato”, “per pelle sensibile”, “per pelle reattiva”, “mild” o simili. Consulta anche l’articolo sui tipi di detergenti.
Leggi anche:
– tipi di detergenti
– funzione e struttura della cute
Riferimenti:
– Corazza M, Lauriola MM, Zappaterra M, Bianchi A, Virgili A. Surfactants, skin cleansing protagonists. J Eur Acad Dermatol Venereol. 2010 Jan;24(1):1-6. doi: 10.1111/j.1468-3083.2009.03349.x. Epub 2009 Jul 14. PMID: 19614860.
– Walters RM, Mao G, Gunn ET, Hornby S. Cleansing formulations that respect skin barrier integrity. Dermatol Res Pract. 2012;2012:495917. doi: 10.1155/2012/495917. Epub 2012 Aug 13. PMID: 22927835; PMCID: PMC3425021.
– Draelos ZD. The science behind skin care: Cleansers. J Cosmet Dermatol. 2018 Feb;17(1):8-14. doi: 10.1111/jocd.12469. Epub 2017 Dec 12. PMID: 29231284.
– Seweryn A. Interactions between surfactants and the skin – Theory and practice. Adv Colloid Interface Sci. 2018 Jun;256:242-255. doi: 10.1016/j.cis.2018.04.002. Epub 2018 Apr 13. PMID: 29685575.



0 commenti